此外,研究人员在多种家猪细胞中检测到SARS-CoV-2靶细胞,这些发现意味着在当前COVID-19大流行期间,有必要仔细评估猫传播新冠的风险,并保持对猪的监视,以防止其在以后的冠状病毒暴发中成为中间宿主。
以上发现来自深圳华大基因研究院等多单位合作在生物预印本平台bioRxiv上的论文“Single-cell screening of SARS-CoV-2 target cells in pets, livestock, poultry and wildlife ”。
该论文的作者团队中多为基因学、兽医学及流行病学专家,通讯作者为华大集团首席执行官、国家基因库执行主任、华大基因研究院院长徐讯,农业基因组学国家重点实验室主任副主任刘欢,华南农业大学校长、国家兽医微生物耐药性风险评估实验室主任刘雅红教授等人。
评估研究新冠病毒动物宿主的易感性对于控制传染病至关重要。研究人员表示,近期的几项研究将穿山甲、猫、狗和仓鼠与SARS-CoV-2的感染和传播联系起来,表明病毒可能在动物中普遍流行,这将对人类构成潜在威胁。
通常情况下,对于宿主动物的易感性推定通过体内试验或接种实验进行,但研究人员指出,这些方法存在满足条件的实验室和人员有限、检测的病毒种类和动物数量有限等问题,而根据病毒进入宿主的机制确定SARS-CoV-2的靶细胞则可缩小假定的中间宿主范围,更加快速准确地确认动物宿主的易感性。
SARS-CoV-2进入宿主细胞是通过病毒刺突糖蛋白(S蛋白)与细胞受体血管紧张素转化酶2(ACE2)结合,以及跨膜丝氨酸蛋白酶2(TMPRSS2)裂解S蛋白而启动的。先前的研究表明,动物组织在细胞组成和基因图谱方面表现出高度的异质性,而ACE2仅在一小部分特定的细胞群体中表达,这使得针对SARS-CoV-2目标细胞的单细胞分析成为本次研究的重点。
研究人员构建了用于牲畜、家禽、宠物和野生动物的单细胞图谱,筛选了144种病毒的受体表达模式,并系统地评估了它们的敏感性。
猫、穿山甲和猪不同器官中SARS-CoV-2靶细胞的筛选
穿山甲和猫都被怀疑是SARS-CoV-2中间宿主。
此前的研究已经从穿山甲中分离出了类似新冠病毒的冠状病毒,并且有研究提出,SARS-CoV-2是起源于穿山甲冠状病毒与蝙蝠冠状病毒的重组;猫也是可疑的中间宿主,因为据此前的报道新冠病毒存在人对猫和猫对猫的传播;家猪是与人紧密接触的动物,此前也有报道称其对新冠病毒敏感。
因此,研究人员针对这三种新冠易感动物的心脏、肝脏、脾脏、肺、肾脏、大肠等组织创建了高质量且全面的单细胞图谱,分别获得了猫、穿山甲和猪的99740、35345和92863个单细胞转录组。

研究人员针对穿山甲、猫、家猪这三种新冠易感动物的心脏、肝脏、脾脏、肺、肾脏、大肠等组织创建了高质量且全面的单细胞图谱
研究人员在猫的肺、眼睑、食道(免疫细胞)和直肠(肠内细胞)中检测到了ACE2和TMPRSS2共同表达细胞。值得注意的是,研究人员发现超过40%的ACE2和TMPRSS2共同表达发生在猫肾近端小管细胞中,约30%的共同表达则发生在猫眼睑上皮细胞中。
在穿山甲中,研究人员发现新冠病毒靶细胞存在于肺内皮细胞、肾脏(内皮细胞、足细胞和近端小管细胞)、肝脏(肝细胞)和脾脏(免疫细胞)中。
在猪体内,ACE2和TMPRSS2主要在肺和肾脏中共同表达。
值得注意的是,研究人员表明,总体而言,猫体内新冠病毒靶细胞的比例远高于穿山甲和猪体内相应细胞类型的比例。
牲畜、家禽、宠物和野生动物肺细胞中SARS-CoV-2靶细胞的筛选
肺是新冠病毒供给的主要靶器官之一,肺炎也是新冠病毒感染的典型症状。为了评估各种物种的肺细胞中ACE2和TMPRSS2的详细表达模式,研究人员进一步生成了家畜(猪、山羊),家禽(鸡、鸽子、鹅、鸭),宠物(猫、狗、仓鼠、蜥蜴),野生动物(穿山甲)的细胞单核库,共获得了123445个细胞。
研究人员表明,与此前的报道一致,SARS-CoV-2在鸡和鸭中的复制较差,在家禽(鸡、鸭、鹅和鸽子)的肺细胞中未发现SARS-CoV-2靶细胞。
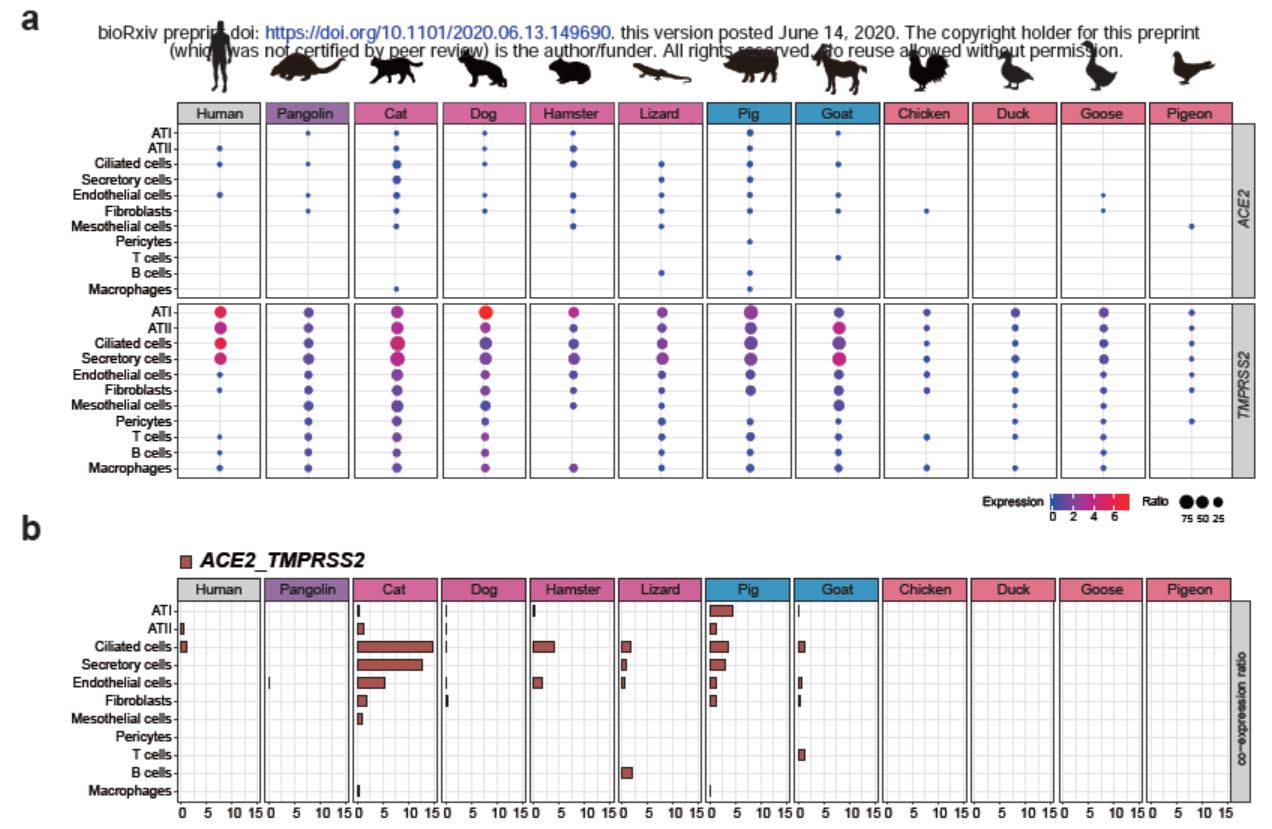
在家禽(鸡、鸭、鹅和鸽子)的肺细胞中未发现SARS-CoV-2靶细胞
在研究人员调查的猫的11种细胞类型中,有8种检测到了SARS-CoV-2靶细胞,其中存在最多新冠病毒靶细胞的两种细胞是纤毛细胞和分泌细胞。
在猪体内,11种细胞类型中的7种中能够观察到ACE2和TMPRSS2的共同表达。
在穿山甲中,研究人员发现一小部分内皮细胞能够共同表达ACE2和TMPRSS2。
在仓鼠中,纤毛细胞是SARS-CoV-2靶细胞最多的细胞类型。
在山羊中,研究人员检测到ACE2和TMPRSS2在AT1受体(血管紧张素1型受体)、成纤维细胞、内皮细胞、纤毛细胞和T细胞中的共同表达。研究人员表明,山羊与猪和人具有高度相似的ACE2氨基酸序列,这表明山羊ACE2也可能具有相似的介导病毒进入宿主细胞的能力。
在蜥蜴体内,研究人员检测到的ACE2和TMPRSS2的共表达主要发生在B细胞中。而在狗的体内,仅有少于0.5%的ACE2和TMPRSS2共表达细胞存在于纤毛细胞和AT2受体(血管紧张素2型受体)中。
为了揭示其他呼吸道病毒的假定肺靶向细胞,研究人员筛选了32种病毒受体的表达模式,以分析来自12个病毒家族的总共29种病毒。
通常,家禽的肺细胞比哺乳动物和爬行动物表达更少类型的病毒受体。例如,人冠状病毒229E的受体ANPEP除了在鸡和鸭肺细胞中表达以外,通常不在家禽肺细胞中表达;SARS(严重急性呼吸综合征)的受体CLEC4G在山羊肺细胞中表达,但在家禽的肺细胞中却不存在。
此外,大多数腺病毒科病毒受体在哺乳动物中优先表达,鼻病毒C受体在人、猫、狗、仓鼠、猪、山羊和鹅的纤毛细胞中优先表达,而呼吸道合胞病毒受体CD209仅存在于人巨噬细胞中。
综上所述,研究人员表示,他们的研究工作首次揭示了不同动物肺中假定的呼吸道病毒靶细胞,这为在单细胞水平上剖析呼吸系统病毒的感染和传播奠定了基础。
猫和猪有更多新冠易感细胞类型,家禽中没有表达
在比较SARS-CoV-2靶向不同物种肺细胞的频率时,研究人员注意到猫的纤毛细胞明显高过其他物种,其被靶向的频率约为13.19%,而猪纤毛细胞仅为3.35%,仓鼠为3.87%。
此外,研究人员在比较猫、穿山甲和猪之间不同器官中SARS-CoV-2靶细胞的比例时也进一步发现,ACE2和TMPRSS2靶细胞在猫中的比例要高得多。例如,在猫的肾近端小管细胞中,ACE2和TMPRSS2共表达细胞的比例高达40%,而穿山甲和猪相应细胞类型的比例分别仅为3%和2%左右。
研究人员还发现,SARS-CoV-2靶细胞广泛分布在猫的消化系统(食道、直肠)、呼吸系统(肺)和泌尿系统(肾脏)内的各个器官之间,这表明猫可能会通过多种途径感染新冠,例如通过饮食感染或通过呼吸系统的空气传播被感染。

SARS-CoV-2靶细胞广泛分布在猫的消化系统、呼吸系统、和泌尿系统、之间
为了突出显示SARS-CoV-2易感细胞类型,研究人员总结了ACE2和TMPRSS2共表达细胞比例高于1%的所有细胞类型,这能够清楚表明,猫和猪比其他物种具有更多的易感细胞类型。
研究人员表明,以上数据说明猫对新冠病毒具有高度易感性,此外,作为伴侣动物,猫与人类的互动显然比穿山甲等更加频繁,因此,研究人员建议在当前的新冠大流行中密切监视猫,对猫作为新冠中间宿主的可能性进行仔细评估。
研究人员还发现,新冠病毒在狗、鸡和鸭中的复制能力很差,但在山羊和蜥蜴肺细胞中检测到了ACE2和TMPRSS2的共表达。
研究数据表明,ACE2和TMPRSS2的共表达在狗的肺细胞中非常罕见,而在家禽的肺细胞(鸡、鸭、鹅和鸽子)中则没有共表达。
此外,SARS-CoV-2的S蛋白不能有效地利用狗和禽类的ACE2,这是因为部分关键氨基酸发生了突变。
此前有研究表明,猪ACE2能够协助新冠病毒进入HeLa细胞,并且研究人员发现SARS-CoV-2靶细胞分布在家猪的肾脏和肺部的多种细胞中,同时此前有过SARS病毒人传猪的报道,因此研究人员认为家猪成为SARS-CoV-2中间宿主的可能性仍需要进一步监测和评估。
值得注意的是,在之前的实验中,鼻内接种SARS-CoV-2后第2天、第4天和第6天,猪的病毒RNA和抗体测试均呈阴性。研究人员认为应谨慎对待猪在未来冠状病毒爆发中的潜在作用,并进行进一步研究。
“病毒进入的红绿灯”系统
在研究不同动物体内新冠靶向细胞情况的同时,为了研究宿主细胞对不同种类病毒的敏感性,研究人员还筛选了144种病毒(代表26个病毒家族)的114种受体在猫、穿山甲和猪的不同器官总以及宠物、牲畜、家禽和野生动物的肺中的表达模式,形成了完整的病毒靶细胞图谱。
为了直观地展示表达病毒受体的细胞的比例,研究人员提出了一种名为“病毒进入的红绿灯”系统,用于将每种细胞类型分配为以下三种状态:红灯、绿灯和黄灯。
简而言之,如果病毒受体的表达量少于该细胞类型的1%,则将分配“红灯”状态(指病毒进入的“红灯”);如果比例在1%到10%之间,则为“黄灯”状态;而如果比例超过10%,则将分配为“绿灯”状态。
有趣的是,研究人员发现狂犬病毒受体NCAM1在猪神经系统的细胞类型中广泛表达,而在非神经组织中很少表达。
此外,该细胞图谱还让研究人员发现水泡性口炎病毒受体UVRAG在猪肺细胞中优先表达。
研究人员称,该项目提供了一种可以根据病毒靶细胞在不同细胞群体之间的分布找出易感宿主的新策略,为今后关于病毒宿主易感性筛选的研究提供了一个新的模型框架,从而甚至可以以无偏见的方式筛查所有现有物种对所有现有病毒的敏感性。
研究人员表示,随着单细胞测序技术的发展以及国际单细胞图谱协作项目的进展,将能够以更快的速度生成更多物种的图谱。